![]()
Andrea Cercek, M.D., Melissa Lumish, M.D., Jenna Sinopoli, N.P., Jill Weiss, B.A., Jinru Shia, M.D., Michelle Lamendola-Essel, D.H.Sc., Imane H. El Dika, M.D., Neil Segal, M.D., Marina Shcherba, M.D., Ryan Sugarman, M.D., Ph.D., Zsofia Stadler, M.D., Rona Yaeger, M.D., et al.
Achtung: Die Patienten in dieser Studie wurden extrem vorgefiltert und hatten alle einen ganz speziellen Gendefekt, den die meisten Darmkrebs Patienten logischerweise nicht haben. Nichtsdestotrotz, sollten sich diese Daten als wahr herausstellen, wäre der Ansatz mit Dostarlimab absolut überlegenswert.
Zusammenfassung
HINTERGRUND
Die neoadjuvante Chemotherapie und Bestrahlung, gefolgt von einer chirurgischen Resektion des Rektums, ist eine Standardbehandlung für lokal fortgeschrittenen Rektumkrebs. Eine Untergruppe des Rektumkarzinoms wird durch einen Mangel an Mismatch-Reparatur verursacht. Da Darmkrebs mit Mismatch-Reparatur-Defizit auf die Blockade des programmierten Todes 1 (PD-1) im Rahmen einer metastasierten Erkrankung anspricht, wurde die Hypothese aufgestellt, dass eine Checkpoint-Blockade bei Patienten mit lokal fortgeschrittenem Rektumkarzinom mit Mismatch-Reparatur-Defizit wirksam sein könnte.
METHODEN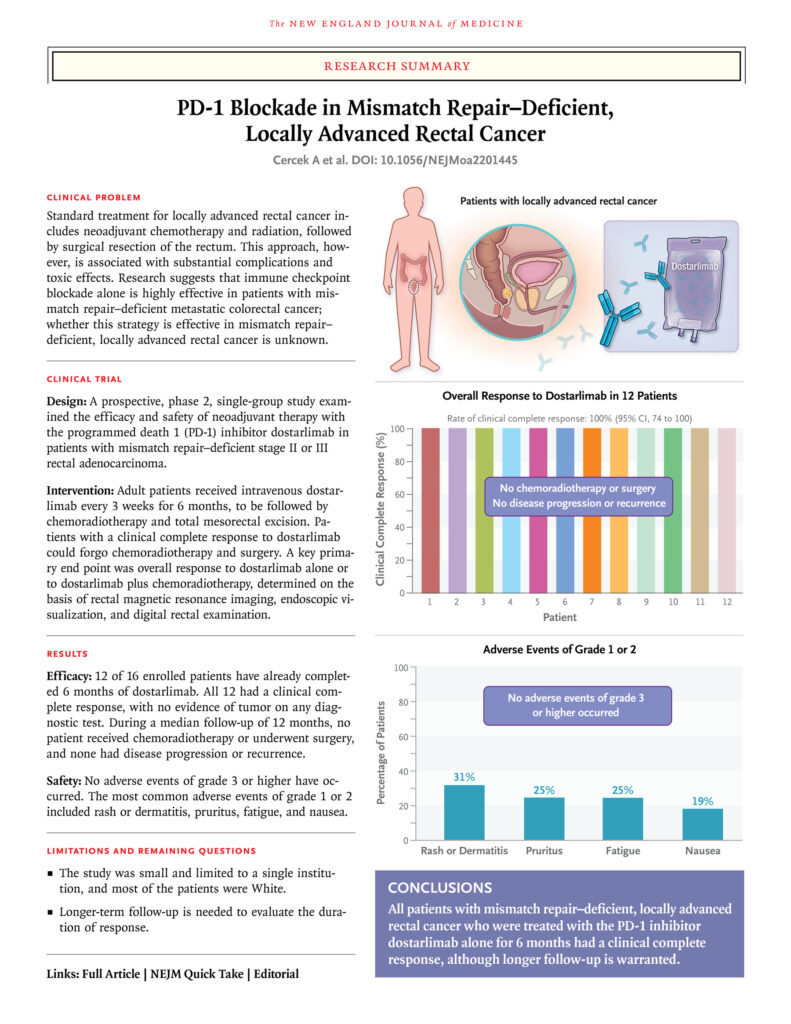
Wir haben eine prospektive Phase-2-Studie initiiert, in der Dostarlimab, ein monoklonaler Anti-PD-1-Antikörper, als Einzelwirkstoff alle drei
Wochen über sechs Monate an Patienten mit Mismatch-Reparatur-defizientem Adenokarzinom des Rektums im Stadium II oder III verabreicht wurde. Auf diese Behandlung sollten eine Standard-Chemoradiotherapie und eine Operation folgen. Patienten, die nach Abschluss der Dostarlimab-Therapie ein klinisch vollständiges Ansprechen zeigten, sollten ohne Chemoradiotherapie und Operation behandelt werden. Die primären Endpunkte sind ein anhaltendes klinisches vollständiges Ansprechen 12 Monate nach Abschluss der Dostarlimab-Therapie oder ein pathologisches vollständiges Ansprechen nach Abschluss der Dostarlimab-Therapie mit oder ohne Chemoradiotherapie sowie das Gesamtansprechen auf die neoadjuvante Dostarlimab-Therapie mit oder ohne Chemoradiotherapie.
ERGEBNISSE
Insgesamt 12 Patienten haben die Behandlung mit Dostarlimab abgeschlossen und wurden mindestens 6 Monate lang nachbeobachtet. Alle 12 Patienten (100 %; 95 % Konfidenzintervall, 74 bis 100) hatten ein klinisch vollständiges Ansprechen, ohne dass ein Tumor in der Magnetresonanztomographie, der 18F-Fluordesoxyglucose-Positronen-Emissions-Tomographie, der endoskopischen Untersuchung, der digitalen rektalen Untersuchung oder der Biopsie nachweisbar war. Zum Zeitpunkt dieses Berichts hatte kein Patient eine Chemoradiotherapie erhalten oder sich einer Operation unterzogen, und während der Nachbeobachtungszeit (zwischen 6 und 25 Monaten) wurden keine Fälle von Progression oder Rezidiv gemeldet. Es wurden keine unerwünschten Ereignisse des Grades 3 oder höher gemeldet.
SCHLUSSFOLGERUNGEN
Das lokal fortgeschrittene Rektumkarzinom mit Mismatch-Reparaturdefizit war sehr empfindlich gegenüber der PD-1-Blockade mit einem einzigen Wirkstoff. Eine längere Nachbeobachtung ist erforderlich, um die Dauer des Ansprechens zu beurteilen. (Finanziert von der Simon and Eve Colin Foundation und anderen; ClinicalTrials.gov Nummer, NCT04165772.)
L okal fortgeschrittenes Rektumkarzinom wird in der Regel mit einer multimodalen Therapie behandelt, die Chemotherapie, Bestrahlung und Operation umfasst. Derzeitige Erkenntnisse unterstützen eine Strategie, die eine neoadjuvante Therapie beinhaltet, bei der auf eine Induktionschemotherapie mit einem Fluoropyrimidin in Kombination mit Oxaliplatin eine Chemoradiotherapie und dann eine Operation folgt.1-3 Dieser Ansatz führt bei bis zu einem Viertel der Patienten zu einem pathologischen vollständigen Ansprechen, ist jedoch bei einem erheblichen Teil der Patienten mit erheblichen Komplikationen und toxischen Wirkungen verbunden – einschließlich Darm-, Harn- und sexueller Funktionsstörungen, Unfruchtbarkeit und veränderter Lebensqualität.4-6 Bei Patienten, die sich einer Operation unterziehen, ist die Resektion des Rektums lebensverändernd und rechtfertigt oft eine permanente Umleitungskolostomie.6,7 Aufgrund der Komplikationen der Operation und der hohen Häufigkeit des pathologischen vollständigen Ansprechens steigt das Interesse an einer organschonenden nichtoperativen Behandlung. Die Verwendung des klinischen vollständigen Ansprechens, das mit einer neoadjuvanten Behandlung erreicht wird, als Surrogat für ein pathologisches vollständiges Ansprechen bietet den Patienten eine nichtoperative Option, die zu einem Überlebensvorteil führt, der mit dem von Patienten vergleichbar ist, die sich einer chirurgischen Resektion unterziehen.8-11
Etwa 5 bis 10 % der Adenokarzinome des Rektums sind Mismatch-Reparatur-defizient, und es hat sich gezeigt, dass diese Tumore schlecht auf Standard-Chemotherapieschemata ansprechen, einschließlich neoadjuvanter Chemotherapie bei lokal fortgeschrittenem Rektumkarzinom.12-14 Die Immun-Checkpoint-Blockade allein hat sich als hochwirksame Erstlinienbehandlung für Patienten mit metastasierendem Darmkrebs mit Mismatch-Reparatur-Defizit sowie für Patienten mit therapierefraktärer Erkrankung erwiesen, mit objektiven Ansprechraten von 33 bis 55 %, klinisch signifikanter Dauerhaftigkeit des Ansprechens und verlängerter Gesamtüberlebenszeit.15-17
Auf der Grundlage der Vorteile, die im Zusammenhang mit metastasierten Erkrankungen beobachtet wurden, stellten wir die Hypothese auf, dass eine alleinige Blockade des programmierten Todes 1 (PD-1) bei lokal fortgeschrittenem Rektumkarzinom mit Mismatch-Reparaturdefizit von Vorteil sein könnte. Um diese Hypothese zu testen, haben wir eine Phase-2-Studie initiiert, um das Gesamtansprechen und die Häufigkeit des anhaltenden klinischen vollständigen Ansprechens auf eine neoadjuvante Behandlung mit Dostarlimab, einem PD-1-Inhibitor, in dieser Patientengruppe zu untersuchen.
Methoden
PATIENTEN
In die Studie wurden Patienten aufgenommen, die mindestens 18 Jahre alt waren und an einem Mismatch-Reparatur-defizienten Rektumkarzinom im Stadium II oder III litten, das anhand klinischer Standardkriterien diagnostiziert worden war. Der Mismatch-Reparatur-Status wurde mit Hilfe eines chromogenen immunhistochemischen Tests zum Nachweis des Verlusts der Expression von MLH1, MSH1, MSH6 und PMS2 bestimmt. Die Stadieneinteilung wurde durch eine Standard-Magnetresonanztomographie (MRT), die nach einem bestimmten Protokoll für Rektumkarzinome durchgeführt wurde, eine Computertomographie (CT) des Brustkorbs, des Abdomens und des Beckens sowie eine Koloskopie bestätigt. Die Positronen-Emissions-Tomographie (PET) wurde gemäß dem aktuellen Studienprotokoll durchgeführt, das zusammen mit dem Volltext dieses Artikels auf NEJM.org verfügbar ist. Die Patienten mussten einen Eastern Cooperative Oncology Group (ECOG) Performance-Status-Score von 0 oder 1 (auf einer 5-Punkte-Skala, wobei höhere Zahlen eine stärkere Behinderung anzeigen) und keine Anzeichen von Fernmetastasen aufweisen. Weitere wichtige Zulassungskriterien waren, dass der Rektumtumor zuvor nicht mit einer Immuntherapie, Chemotherapie oder Bestrahlung behandelt worden war und dass keine aktive Autoimmunerkrankung, aktive Infektionskrankheit oder kürzlich (innerhalb der letzten 7 Tage) eine immunsuppressive Therapie durchgeführt wurde.
STUDIENAUFBAU
In dieser prospektiven Ein-Gruppen-Phase-2-Studie wurde neoadjuvantes Dostarlimab in einer Dosis von 500 mg alle drei Wochen über sechs Monate (neun Zyklen) intravenös verabreicht, gefolgt von einer Standard-Strahlentherapie (Gesamtdosis von 5040 cGy in 28 Fraktionen) mit gleichzeitiger Verabreichung von Capecitabin in Standarddosen und anschließender vollständiger mesorektaler Exzision. Patienten, die nach Abschluss der Anti-PD-1-Induktionstherapie oder der Chemoradiotherapie ein klinisch vollständiges Ansprechen (wie unten definiert) zeigten, wurden anschließend einer nichtoperativen Nachuntersuchung unterzogen (Abb. S1 im ergänzenden Anhang, verfügbar auf NEJM.org).
Das klinische Ansprechen der Patienten wurde anhand endoskopischer und digitaler rektaler Untersuchungen zu Studienbeginn (vor der Behandlung), nach 6 Wochen, nach 3 Monaten, nach 6 Monaten und dann alle 4 Monate nach Behandlungsbeginn beurteilt. T2-gewichtete und diffusionsgewichtete MRT-Untersuchungen des Rektums,18 18F-Fluordesoxyglukose (FDG)-PET und CT-Untersuchungen des Brustkorbs, des Abdomens und des Beckens wurden zu Beginn der Behandlung, nach drei Monaten, nach sechs Monaten und dann alle vier Monate nach Behandlungsbeginn durchgeführt. Tumorbiopsien wurden bei jeder Endoskopie durchgeführt. Alle Untersuchungen sollten frühzeitig durchgeführt werden, wenn die Patienten klinische Symptome einer Progression aufwiesen.
Das Ansprechen des Tumors wurde anhand der T2-gewichteten und diffusionsgewichteten MRT des Rektums, der endoskopischen Beurteilung und der digitalen rektalen Untersuchung bestimmt.19 Ein klinisch vollständiges Ansprechen wurde definiert als das Fehlen einer Restkrankheit bei der digitalen und endoskopischen rektalen Untersuchung sowie als das Fehlen einer Restkrankheit bei der rektalen MRT, ohne eingeschränkte Diffusion bei der T2-gewichteten Bildgebung.
ÜBERWACHUNG DER STUDIE
Dies ist eine vom Prüfarzt initiierte Studie. Das Protokoll wurde vom institutionellen Prüfungsausschuss des Memorial Sloan Kettering Cancer Center genehmigt. Alle Patienten haben vor der Teilnahme an der Studie eine schriftliche Einverständniserklärung gemäß den Grundsätzen der Deklaration von Helsinki abgegeben. Die Autoren bürgen für die Vollständigkeit und Genauigkeit der Daten sowie für die Einhaltung des Studienprotokolls.
ENDPUNKTE
Im Rahmen der Studie werden zwei primäre Endpunkte untersucht, wobei eine Rekrutierung von 30 Patienten geplant ist. Ein Endpunkt ist das anhaltende klinische vollständige Ansprechen 12 Monate nach Abschluss der Dostarlimab-Therapie (bei Patienten, die nicht operiert werden) oder das pathologische vollständige Ansprechen (bei Patienten, die operiert werden) nach Abschluss der Dostarlimab-Therapie mit oder ohne Chemoradiotherapie. Ein pathologisches vollständiges Ansprechen wurde im Protokoll als Abwesenheit von Restkrebs bei der histologischen Untersuchung der chirurgischen Proben definiert. Der andere Endpunkt ist das Gesamtansprechen auf die neoadjuvante Dostarlimab-Therapie mit oder ohne Chemoradiotherapie. Hier wird nur über den zweiten Endpunkt berichtet. Das Gesamtansprechen wurde auf der Grundlage der T2-gewichteten und diffusionsgewichteten MRT des Rektums, der endoskopischen Darstellung und der digitalen rektalen Untersuchung bestimmt. Das Gesamtansprechen wurde im Protokoll als progrediente Erkrankung, stabile Erkrankung, teilweises Ansprechen, nahezu vollständiges Ansprechen oder vollständiges Ansprechen definiert (weitere Einzelheiten sind im Protokoll enthalten).
PATHOLOGISCHE UND GENOMISCHE ANALYSEN
Formalinfixierte, in Paraffin eingebettete Tumorproben aus Biopsien, die während der Studie durchgeführt wurden, wurden mit Hämatoxylin und Eosin gefärbt und von einem geschulten Pathologen begutachtet, der die Proben visuell beurteilte, um die Diagnose zu bestätigen, die allgemeinen histologischen Merkmale zu identifizieren und den Prozentsatz der lebensfähigen Tumorzellen in jeder Tumorprobe zu schätzen. Der Mismatch-Reparatur-Status wurde mit Hilfe eines chromogenen immunhistochemischen Assays zum Nachweis des Verlusts der Expression von MLH1, MSH1, MSH6 und PMS2 bestimmt.
Tumorspezifische und Keimbahn-umfassende Genomanalysen wurden mit Hilfe von Memorial Sloan Kettering-Integrated Mutation Profiling of Actionable Cancer Targets (MSK-IMPACT), einem Sequenzierungstest der nächsten Generation, durchgeführt. Dieser von der Food and Drug Administration zugelassene Assay erkennt somatische und Keimbahnveränderungen in mehr als 400 Genen und bewertet die Mutationslast des Tumors. Alle Patienten, die sich einer umfassenden molekularen Analyse auf somatische tumorspezifische Veränderungen oder einer Analyse bekannter erblicher Veränderungen unterzogen, gaben eine zusätzliche schriftliche Einwilligung, die sich auf diese Analysen bezog.
Formalinfixierte, in Paraffin eingebettete Biopsieschnitte wurden auch mit Hilfe einer quantitativen Immunfluoreszenzanalyse ausgewertet, die für die gleichzeitige Messung von DAPI (4′,6-Diamidin-2-Phenylindol) für alle Zellen, Zytokeratin für Tumor- und normale Darmepithelzellen (Klon AE1/AE3, Dako), CD20+ B-Lymphozyten (Klon L26, M0755; Dako), Programmed Death Ligand 1 (PD-L1) (Klon E1L3N, CST) und CD8+ T-Lymphozyten (Klon C8/144B, M7103; Dako). Die Konzentrationen der Marker wurden in ausgewählten Gewebekompartimenten gemessen und als quantitative Immunfluoreszenz-Scores auf der Grundlage willkürlicher Fluoreszenzeinheiten ausgedrückt. Einzelheiten sind im Abschnitt Methoden im ergänzenden Anhang aufgeführt.
STATISTISCHE ANALYSE
Wir bewerteten die Gesamtansprechrate anhand einer Einstichprobenhypothese; die zu prüfende Nullhypothese war, dass der Prozentsatz der Patienten mit einem Gesamtansprechen weniger als 25 % betragen würde. Um die Nullhypothese erfolgreich zu verwerfen, müssten am Ende der ersten Phase (nach Aufnahme von 15 Patienten) 6 oder mehr Patienten mit einer Gesamtansprechrate und am Ende der zweiten Phase (nach Aufnahme von 30 Patienten) 11 oder mehr Patienten mit einer Gesamtansprechrate vorliegen. Diese Entscheidungsregel würde zu einer Fehlerquote vom Typ I von 6 % führen, wenn 25 % der Patienten ein Gesamtansprechen hätten, und würde der Studie eine Aussagekraft von 84 % verleihen, wenn 50 % ein Gesamtansprechen hätten. Die Nullhypothese wurde auf der Grundlage einer Studie von Seligmann et al. aufgestellt, in der das beobachtete Ansprechen auf eine Chemotherapie bei Patienten mit Mismatch-Reparatur-defizientem Rektumkarzinom 7 % betrug (8 von 115 Patienten).20 Wir geben die Ergebnisse bekannt, ohne die vollständige Rekrutierung abzuwarten, da das zweite Kriterium für die Entscheidungsregel (≥11 Patienten mit einem Gesamtansprechen) bereits erfüllt ist.
Die Binomialproportionen werden mit einem exakten 95 %-Konfidenzintervall angegeben. Quantitative Immunfluoreszenz-Scores für pathologische Proben, die bei Studienbeginn, während der Behandlung und während der Nachbeobachtung gewonnen wurden, wurden mit Hilfe des Mann-Whitney-Tests verglichen. Die statistische Analyse und die grafische Darstellung wurden mit der Software GraphPad Prism, Version 9.0.2 (GraphPad Software), durchgeführt. P-Werte von weniger als 0,05 wurden als Hinweis auf statistische Signifikanz betrachtet.
Ergebnisse
PATIENTEN

Demographic and Disease Characteristics of the Patients at Baseline.
Demografische und krankheitsbezogene Merkmale der Patienten bei Studienbeginn. Insgesamt wurden 16 Patienten in die Studie aufgenommen und behandelt (Tabelle 1). Von diesen Patienten wurden 12 länger als 6 Monate in die Studie aufgenommen und haben die neun geplanten Zyklen (6 Monate) von Dostarlimab abgeschlossen. Die mediane Nachbeobachtungszeit von der Aufnahme in die Studie bis zum Erreichen der klinischen Daten beträgt bei den 12 Patienten 12 Monate (Spanne 6 bis 25). Die übrigen 4 Patienten haben mindestens eine Dosis Dostarlimab erhalten und werden weiterhin behandelt. Das Durchschnittsalter aller eingeschlossenen Patienten liegt bei 54 Jahren (Spanne 26 bis 78), und 62 % sind Frauen. Alle 16 Patienten erfüllten die Zulassungskriterien, und kein Patient hat sich aus der Studie zurückgezogen. Von den 16 Patienten befinden sich 15 im klinischen Stadium III und 1 Patient im klinischen Stadium II der Erkrankung. Die häufigsten Symptome waren rektale Blutungen (bei 88 % der Patienten), Verstopfung (bei 31 %) und Unterleibsschmerzen (bei 25 %) (Tabelle S1).
TUMORMERKMALE
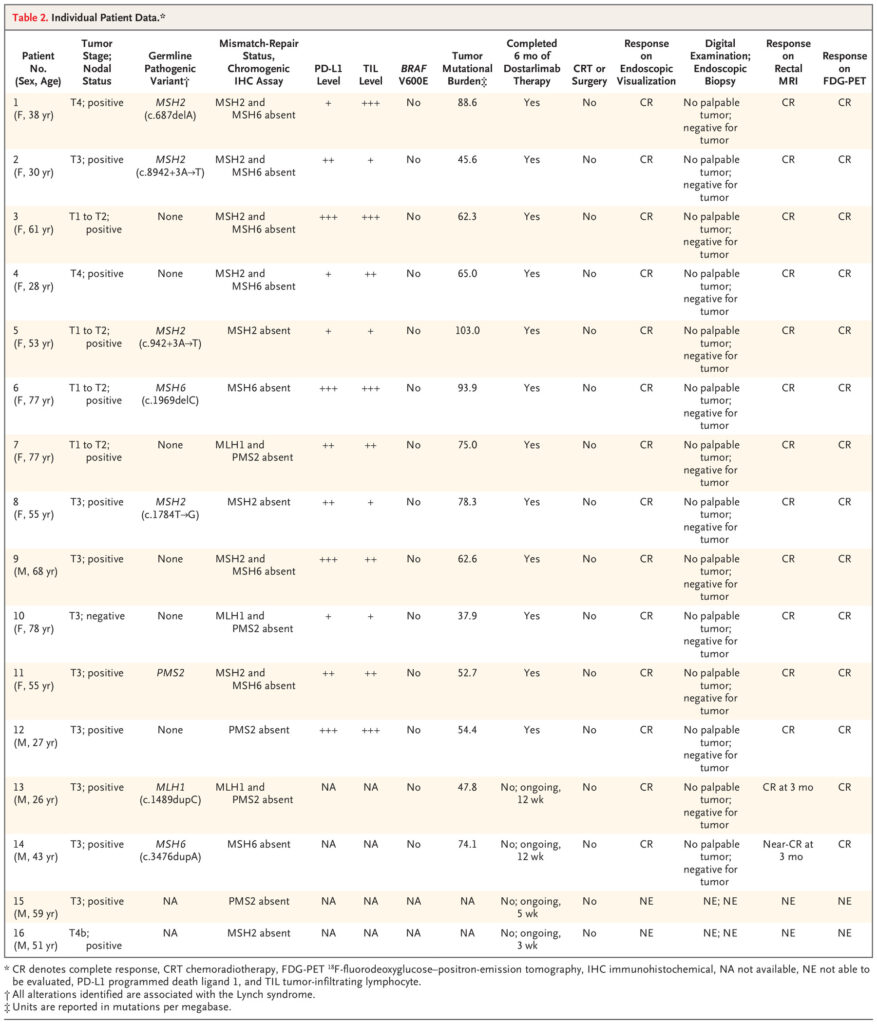
Individual Patient Data.
Individuelle Patientendaten.
Die Mutationsanalyse der Tumorproben mittels Next-Generation-Sequenzierung bestätigte die Mikrosatelliteninstabilität bei allen 14 Patienten, bei denen der Test durchgeführt wurde, und ergab eine hohe Tumormutationslast, die von 37,9 bis 103,0 Mutationen pro Megabasis (Mittelwert 60,0) reichte. Die BRAF-V600E-Mutation war bei allen 14 Patienten nicht vorhanden (Tabelle 2 und Tabelle S2).
Bei keinem der Patienten war in der Familiengeschichte das Lynch-Syndrom bekannt. Bei der Keimbahnanalyse wurden bei 57 % der Patienten (8 von 14 Patienten) pathogene Genomveränderungen festgestellt; alle Veränderungen sind mit dem Lynch-Syndrom assoziiert. Am häufigsten waren Veränderungen in MSH2, die bei 4 der 8 Patienten auftraten; pathogene Veränderungen in MSH6, MLH1 und PMS2 waren ebenfalls vorhanden (Tabelle 2).
EFFIZIENZ
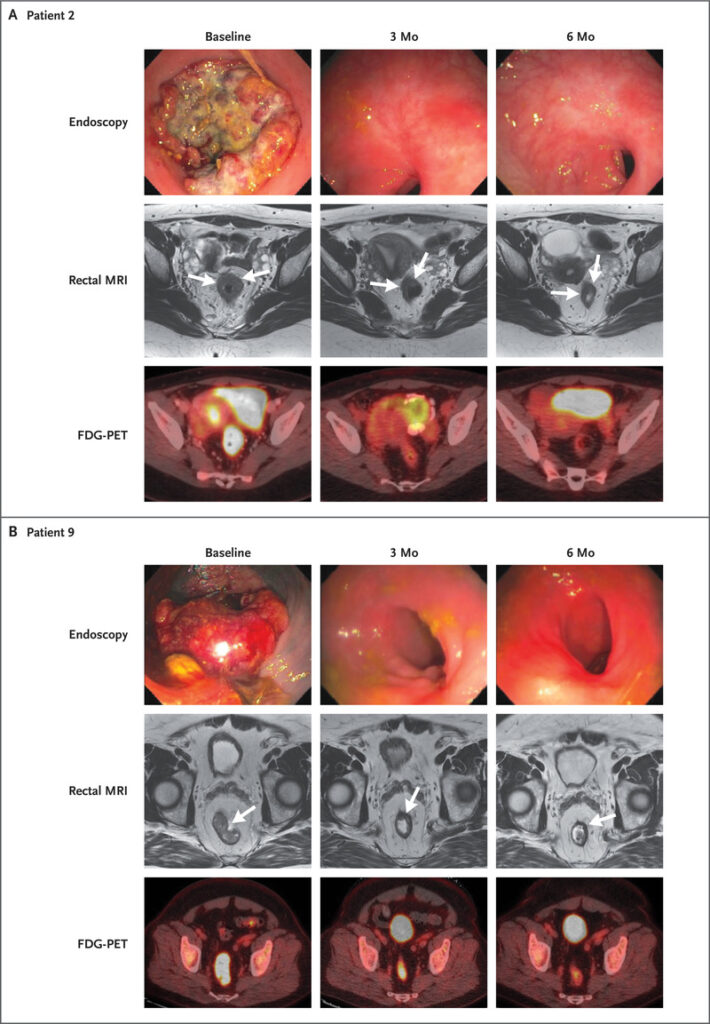
Evolution of Endoscopic and Radiographic Response in Representative Patients Treated with Dostarlimab.
Entwicklung des endoskopischen und röntgenologischen Ansprechens bei repräsentativen Patienten, die mit Dostarlimab behandelt wurden.
Die Kriterien für den primären Endpunkt des Gesamtansprechens auf eine neoadjuvante Dostarlimab-Therapie mit oder ohne Chemoradiotherapie wurden erfüllt. Der Prozentsatz der Patienten mit einem klinisch vollständigen Ansprechen betrug 100 % (95 % Konfidenzintervall [KI], 74 bis 100) bei 12 konsekutiven Patienten, die die 6-monatige Therapie abgeschlossen haben (Abbildung 1, Tabelle 2 und Abb. S2). Nach Abschluss der Therapie nach 6 Monaten betrug die mediane Zeit bis zur rektalen MRT 16 Tage (Bereich 8 bis 26) und die mediane Zeit bis zur Endoskopie 20 Tage (Bereich 14 bis 28).
Während der medianen Nachbeobachtungszeit von 12 Monaten hat kein Patient eine Chemoradiotherapie erhalten, und kein Patient hat sich einer chirurgischen Resektion unterzogen. Da sich keiner der 12 Patienten, die eine 6-monatige Dostarlimab-Therapie abgeschlossen haben, einer Operation unterzogen hat, ist eine Bewertung des pathologischen vollständigen Ansprechens nicht möglich. Keiner der Patienten hatte einen Krankheitsfortschritt oder ein Rezidiv, und alle 16 eingeschlossenen Patienten sind am Leben (Tabelle 2 und Tabelle S2).
Der primäre Endpunkt, bei dem es um die Dauerhaftigkeit des Ansprechens geht (anhaltendes klinisches vollständiges Ansprechen nach 12 Monaten), wird nicht abschließend berichtet. Bislang haben 4 Patienten nach Abschluss der Behandlung mit Dostarlimab allein ein Jahr lang ein anhaltendes klinisches vollständiges Ansprechen gezeigt (Tabelle S2).
Das therapeutische Ansprechen erfolgte rasch, wobei die Symptome bei 81 % der Patienten innerhalb von 9 Wochen nach Beginn der Behandlung mit Dostarlimab verschwanden. Zum Zeitpunkt der 3-Monats-Bewertung hatten 5 Patienten ein vollständiges endoskopisches Ansprechen, aber nur 2 Patienten hatten ein vollständiges radiologisches Ansprechen (Abb. S3 und Tabellen S1 und S2).
SICHERHEIT
Unerwünschte Ereignisse jeglichen Grades traten bei 12 der 16 Patienten auf (75 %; 95 % CI, 48 bis 92). Es wurden keine unerwünschten Ereignisse des Grades 3 oder höher gemeldet. Zu den häufigsten unerwünschten Ereignissen des Grades 1 oder 2 gehörten Hautausschlag oder Dermatitis (bei 31 % der Patienten), Juckreiz (bei 25 %), Müdigkeit (bei 25 %) und Übelkeit (bei 19 %). Schilddrüsenfunktionsanomalien traten bei 1 Patienten (6 %) auf (Tabelle S3).
BIOMARKER FÜR LANGZEITREAKTIONEN
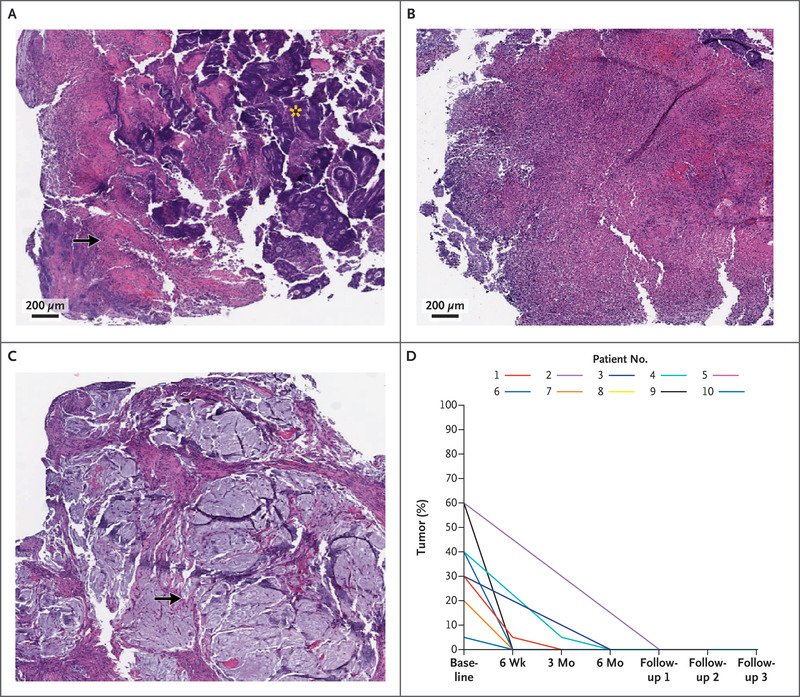
Biopsy Specimens of the Rectum before and after PD-1 Blockade and Viable Tumor Cell Content.
Biopsieproben des Rektums vor und nach PD-1-Blockade und Gehalt an lebensfähigen Tumorzellen.
Endoskopische Biopsien wurden zu Beginn der Studie und während der visuellen Inspektion des Tumoransprechens nach 6 Wochen, nach 3 Monaten, nach 6 Monaten und dann alle 4 Monate durchgeführt. Patienten, die nach 6 Monaten Dostarlimab-Therapie ein klinisch vollständiges Ansprechen hatten und über Gewebe verfügten, das ausgewertet werden konnte, wiesen auch bei der endoskopischen Biopsie keine Anzeichen für einen Tumor auf, wobei die Mehrheit der Patienten bereits 6 Wochen nach Beginn der Therapie keine Anzeichen für einen lebensfähigen Tumor aufwies (Abbildung 2). Die longitudinalen endoskopischen, pathologischen und radiologischen Daten für jeden Patienten sind in Abbildung S4 dargestellt.
Veränderungen der Immunkontextur nach PD-1-Blockade in Rektumtumoren und Schleimhaut.
Die mittels quantitativer Multiplex-Immunfluoreszenzanalyse ausgewerteten Tumorproben zeigten eine variable PD-L1-Proteinexpression mit
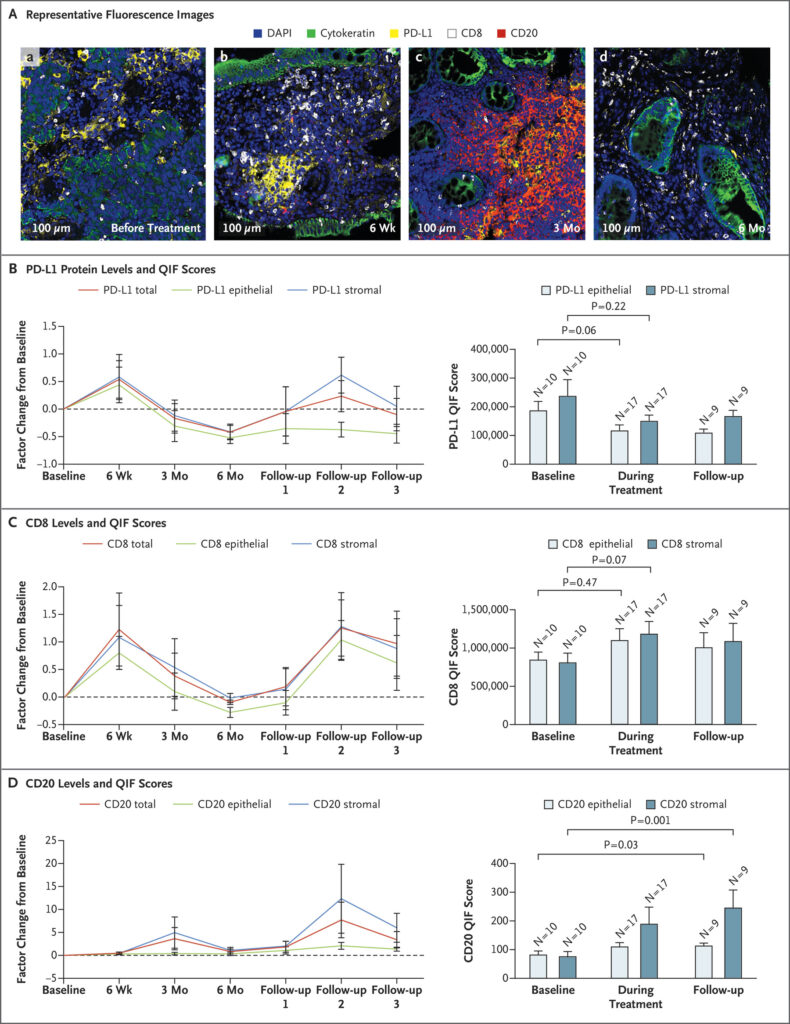
Immune Contexture Changes after PD-1 Blockade in Rectal Tumors and Mucosa.
höheren Werten in Zytokeratin-negativen Stromazellen als in Zytokeratin-exprimierenden Krebszellen sowie eine lymphozytäre Infiltration, die mit CD8- oder CD20-exprimierenden Zellen angereichert war. PD-L1-Protein und CD8+ T-Lymphozyten waren zu Beginn der Behandlung vorhanden; die Konzentrationen von beiden stiegen 6 Wochen nach der Verabreichung von Dostarlimab im Tumor und im normalen Epithelgewebe sowie im Stromagewebe an, sanken jedoch vorübergehend von 3 bis 6 Monaten während der Behandlung und kehrten dann nach 6 Monaten zu höheren Konzentrationen in der tumorfreien Rektumschleimhaut zurück. CD20+ B-Lymphozyten bildeten knotige Aggregate, vorwiegend in den stromalen Bereichen, die mit tertiären lymphatischen Strukturen übereinstimmten. Die Konzentrationen dieser Aggregate stiegen nach sechswöchiger Therapie allmählich an und erreichten sechs Monate nach Abschluss der Dostarlimab-Therapie Werte, die sechs- bis zehnmal so hoch waren wie die Ausgangswerte (Abbildung 3).
Serielle FDG-PET-Scans, die zu Beginn, nach drei Monaten, nach sechs Monaten und dann alle vier Monate durchgeführt wurden, um das Ansprechen des Tumors auf die PD-1-Blockade weiter zu bewerten, zeigten eine Entwicklung der Tumorauslöschung, die derjenigen bei der pathologischen Untersuchung und der Genomanalyse ähnelte. Die maximalen standardisierten Aufnahmewerte waren bei allen Patienten bereits 3 Monate nach Beginn der Dostarlimab-Therapie auf das Hintergrundniveau gesunken. Bei allen Patienten, die die 6-monatige Behandlung abgeschlossen hatten, war der Tumor im FDG-PET vollständig verschwunden (Abb. S5).
Diskussion
In dieser Studie mit Patienten mit Mismatch-Reparatur-defizientem, lokal fortgeschrittenem Rektumkarzinom führte die Behandlung mit der neoadjuvanten PD-1-Blockade allein zu einem klinisch vollständigen Ansprechen – gemessen durch die Kombination aus rektaler MRT, visueller endoskopischer Inspektion und digitaler rektaler Untersuchung – bei allen 12 Patienten, die mindestens 6 Monate lang nachuntersucht wurden. Die Vollständigkeit dieses Ansprechens wird durch das Fehlen eines Resttumors bei seriellen endoskopischen Biopsien und die Auflösung der FDG-Aufnahme bei PET-Scans bestätigt.
In unserer Studie ermöglichte es uns die Eliminierung der Tumore nach sechsmonatiger PD-1-Blockade, sowohl auf eine Chemoradiotherapie als auch auf eine Operation zu verzichten und nur eine Beobachtung durchzuführen. Chirurgie und Bestrahlung können dauerhafte Auswirkungen auf die Fruchtbarkeit, die sexuelle Gesundheit sowie die Darm- und Blasenfunktion haben.4-7,21 Die Auswirkungen auf die Lebensqualität sind erheblich, insbesondere bei Patienten, bei denen eine Standardbehandlung das Kinderwunschpotenzial beeinträchtigen würde. Da die Häufigkeit von Rektumkarzinomen bei jungen Erwachsenen im gebärfähigen Alter zunimmt, könnte die PD-1-Blockade, die eine Chemoradiotherapie und eine Operation überflüssig macht, in dieser Altersgruppe von besonderem Nutzen sein.22
Die neoadjuvante Immuntherapie wurde bei verschiedenen soliden Tumoren23-26 getestet, darunter auch bei solchen, die bekanntermaßen auf Checkpoint-Blockaden im Zusammenhang mit einer metastasierten Erkrankung ansprechen, wie nicht-kleinzelliger Lungenkrebs (NSCLC), Urothelkarzinom und Melanom. Die bei diesen Tumorarten beobachtete Aktivität war nicht annähernd so hoch wie die, die wir bei Patienten mit Mismatch-Reparatur-defizientem Rektumkarzinom beobachtet haben. Ein Grund dafür könnte sein, dass wir eine sechsmonatige Immuntherapie verabreicht haben, während in den anderen Studien eine kürzere Exposition gegenüber der Checkpoint-Blockade untersucht wurde. Es hat sich gezeigt, dass sich das Ansprechen auf eine Immuntherapie bei Mismatch-Reparatur-defizienten Tumoren eher über Monate als über Wochen entwickelt.27 Wir haben jedoch bei vielen der Patienten in unserer Studie nach nur 3 Monaten Behandlung zumindest ein nahezu vollständiges Ansprechen beobachtet. In einer Studie mit Patienten mit nicht-kleinzelligem Lungenkrebs (NSCLC) führten zwei Dosen der PD-1-Blockade zu einer Ansprechrate von 10 %, und in einer Studie mit Patienten mit Melanom sprachen 52 % auf die Immuntherapie allein an.24,28 In einer Pilotstudie, in der Patienten mit Mismatch-Reparatur-defizientem Dickdarmkrebs vor der Operation eine Einzeldosis Ipilimumab und zwei Dosen Nivolumab erhielten, sprachen 50 % der Patienten an.29 In einer Studie, in der Patienten mit therapierefraktärem Mismatch-Reparatur-defizientem Dickdarmkrebs im Frühstadium entweder mit Toripalimab (einem PD-1-blockierenden Antikörper) plus Celecoxib oder Toripalimab-Monotherapie über drei Monate behandelt wurden, kam es bei etwa 55 % der Patienten zu einem bildgebungsbasierten Ansprechen.30 In all diesen Studien wurde jedoch bei allen Patienten eine chirurgische Resektion durchgeführt, wodurch die mit diesem Verfahren verbundenen langfristigen Komplikationen auftraten.
Eine wichtige Frage ist, warum diese lokalisierten Mismatch-Reparatur-defizienten Rektumtumoren so viel besser ansprechen als metastasierende kolorektale Tumoren. In einer Studie mit Patienten mit metastasierter Erkrankung, die zuvor keine Behandlung erhalten hatten, lag die Rate der bildgebungsbasierten vollständigen Reaktion von Mismatch-Reparatur-defizienten kolorektalen Tumoren bei 11,1 %, obwohl bei Studienbeginn molekulare Merkmale vorlagen, die denen der in unserer Studie untersuchten Tumoren ähnelten.15 Eine Erklärung, die sich für Tumoren des Gastrointestinaltrakts anbietet, ist der mögliche Einfluss des Darmmikrobioms. Eine wachsende Zahl von Veröffentlichungen unterstützt die immunmodulatorische Rolle bestimmter Bakterienspezies bei der Verstärkung der antitumoralen Immunantwort, die durch die Checkpoint-Blockade potenziert wird.31-33 Eine Studie zur neoadjuvanten Checkpoint-Blockade bei NSCLC zeigte, dass eine Fülle von Ruminococcus- und Akkermansia-Spezies im Darm mit einer größeren pathologischen Reaktion verbunden war.34 Es wurde festgestellt, dass Fusobacterium nucleatum in Mismatch-Reparatur-defizienten Tumoren mit einer immunresponsiven Tumormikroumgebung assoziiert ist.35 Wir spekulieren, dass zusätzlich zu dem tumorzelleigenen Faktor, der das Ansprechen auf die PD-1-Blockade bewirkt (nämlich die extrem hohe Tumormutationslast, die mit dem Mismatch-Reparatur-Defizit verbunden ist), ein tumorexterner Faktor, wie das Mikrobiom, dieses außergewöhnlich gute Ansprechen bewirken könnte. Tumorzelleigene Merkmale, die über die Mutationslast des Tumors hinausgehen – wie Klonalität, Aneuploidie und Mutationsklasse,36-38 die nachweislich das Ansprechen auf eine Immuntherapie beeinflussen – könnten die Unterschiede im Ansprechen zwischen lokalisierten und metastasierten Erkrankungen beeinflussen.
Die Entwicklung der lokalen Immunantwort zeigte eine erhebliche anfängliche Zunahme von PD-L1-positiven und CD8+ T-Lymphozyten, gefolgt von einem Rückgang auf ein Niveau, das unter dem der Vorbehandlung lag, und zwar in demselben Zeitraum, in dem das vollständige Ansprechen erreicht wurde. Nach Abschluss der Behandlung wurde eine Neubesiedlung mit PD-L1-positiven Zellen festgestellt, vor allem im Stroma, in Verbindung mit einer Vermehrung der CD8+ T-Lymphozyten und einem deutlichen Anstieg der CD20+ B-Lymphozyten innerhalb der tertiären lymphoiden Strukturen (Daten nicht gezeigt). Bei Melanomen wurde die Koexistenz von CD8+ T-Lymphozyten und CD20+ B-Lymphozyten und die Entwicklung tertiärer lymphoider Strukturen mit einem verbesserten klinischen Nutzen der Checkpoint-Blockade in Verbindung gebracht.39
Obwohl die Ergebnisse unserer Studie vielversprechend sind, insbesondere angesichts der Tatsache, dass 12 konsekutive Patienten alle ein klinisches vollständiges Ansprechen hatten, ist die Studie klein und repräsentiert die Erfahrung einer einzigen Einrichtung. Diese Ergebnisse müssen in einer größeren prospektiven Kohorte reproduziert werden, die ein Gleichgewicht zwischen akademischen und kommunalen Praktiken herstellt und die Teilnahme von Patienten mit unterschiedlichem rassischen und ethnischen Hintergrund gewährleistet.
Sobald Daten über die Dauer des vollständigen Ansprechens – der andere primäre Endpunkt der Studie – vorliegen, wird sich die Frage stellen, ob dieser Ansatz langfristig alle oder die meisten Patienten vor einer chirurgischen Resektion bewahren wird. Bislang haben 4 der 13 Patienten, die unsere vorgegebenen Kriterien für den Endpunkt der Dauer des Ansprechens erfüllen mussten, ein anhaltendes klinisches vollständiges Ansprechen für mehr als 1 Jahr nach Abschluss der Dostarlimab-Therapie gezeigt. In einer Studie mit Patienten mit metastasierenden Mismatch-Reparatur-defizienten Tumoren, die nach einer Behandlung mit einer PD-1-Blockade objektiv ansprachen, lag die Dauer des Ansprechens nach 30 Monaten bei über 75 %40. Diese Ergebnisse stimmen uns optimistisch, dass die Krankheitsremission im Rahmen einer neoadjuvanten Therapie dauerhaft sein wird. Sobald diese Daten ausgereift sind, können wir uns vorstellen, dass die PD-1-Blockade im Rahmen einer neoadjuvanten Behandlung auch bei anderen Tumoren mit Mismatch-Reparatur-Defizit untersucht wird, z. B. bei lokalisierten Bauchspeicheldrüsen-, Magen- und Prostatakrebsen; dies könnte die Tür für einen immunoablativen Ansatz öffnen, der eine Vielzahl von Tumorarten einbezieht, die mit einem Mismatch-Reparatur-Defizit bei Patienten mit metastasierter Erkrankung einhergehen. Falls ein lokales oder entferntes Rezidiv beobachtet wird, kann zusätzlich zur Checkpoint-Blockade eine kombinierte Chemotherapie oder Bestrahlung gerechtfertigt sein.
In unserer Studie war Dostarlimab als Einzelwirkstoff bei lokal fortgeschrittenem Rektumkarzinom mit Mismatch-Reparaturdefizit bemerkenswert wirksam und führte bei allen 12 Patienten, die die Behandlung bis heute abgeschlossen haben, zu einem vollständigen klinischen Ansprechen. Die Studie bietet auch einen Rahmen für die Bewertung hochwirksamer Krebstherapien im neoadjuvanten Kontext, bei dem Patienten möglicherweise von Chemoradiotherapie und Operation verschont bleiben, während ihr Tumor zu einem Zeitpunkt behandelt wird, an dem er am ehesten anspricht – nämlich bevor er anderen Wirkstoffen ausgesetzt wird, die für Zellen mit einem resistenten Phänotyp selektieren könnten.
Originalartikel aus >> https://www.nejm.org/doi/full/10.1056/NEJMoa2201445